UE oficjalnie wydała zgodę na awaryjne stosowanie tabletki przeciw COVID-19 firmy Merck
Organ nadzorujący leki Unii Europejskiej oficjalnie wydał zgodę na stosowanie tabletki przeciw COVID-19 opracowanej przez firmę Merck.
Zielone światło
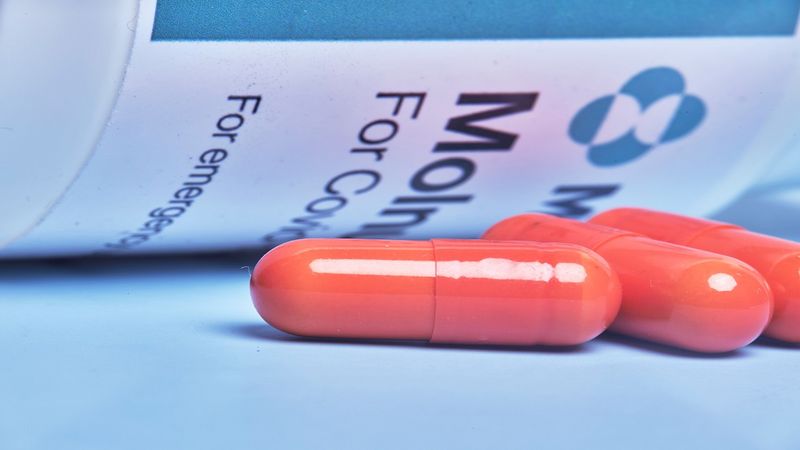
Europejska Agencja Leków (EMA) ogłosiła, że molnupirawir (Lagevrio lub MK 4482) może być stosowany w sytuacjach kryzysowych u osób dorosłych z COVID-19, które nie wymagają dodatkowego tlenu i są w grupie zwiększonego ryzyka rozwoju ciężkiego COVID-19.
Tabletka przeciwwirusowa hamuje replikację niektórych wirusów RNA. Leczenie polega na przyjmowaniu dwóch kapsułek dziennie przez pięć dni. Najlepiej sprawdza się we wczesnych stadiach choroby.
EMA wydała zgodę na stosowanie środka w wyjątkowych przypadkach. Lek należy podać zaraz po rozpoznaniu COVID-19, najpóźniej w ciągu pięciu dni od wystąpienia pierwszych objawów.

Wstępne badania
Pierwsze badania nad molnupirawirem wykazały, że leczenie o połowę zmniejsza ryzyko hospitalizacji i zgonu. W badaniu 385 pacjentów wysokiego ryzyka COVID-19 otrzymywało dwie dzienne dawki leku, a 377 otrzymywało placebo.
Po miesiącu 7,3% pacjentów przyjmujących molnpirawir było hospitalizowanych, w porównaniu do 14,1 w grupie placebo. W pierwszej grupie nie zgłoszono żadnych zgonów, z kolei w drugiej zmarło osiem osób.

Konkurencyjny środek
EMA wydała zgodę „w świetle rosnących wskaźników infekcji i zgonów z powodu COVID-19 w całej UE”. W kilku europejskich krajach w ostatnim czasie przybyła drastyczna liczba chorych.
W międzyczasie UE przygląda się także Paxlovid, konkurencyjnej pigułce opracowanej przez Pfizer. Wstępne dane sugerują, że stosowanie środka w leczeniu osób wysokiego ryzyka zmniejsza prawdopodobieństwo hospitalizacji i zgonu o 89 procent.